Classement
Contenu populaire
Affichage du contenu avec la meilleure réputation depuis le 09/11/2023 dans toutes les zones
-
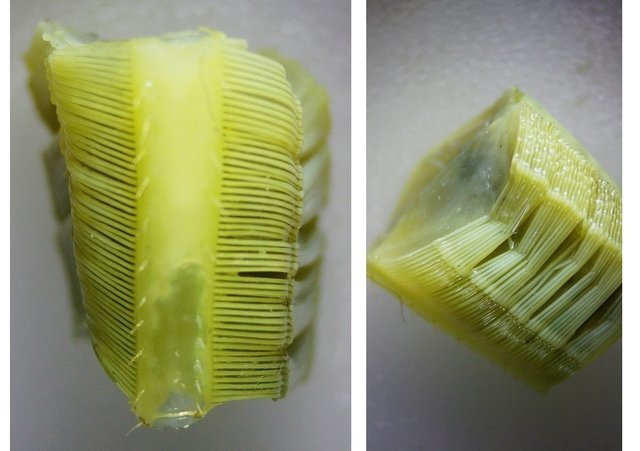
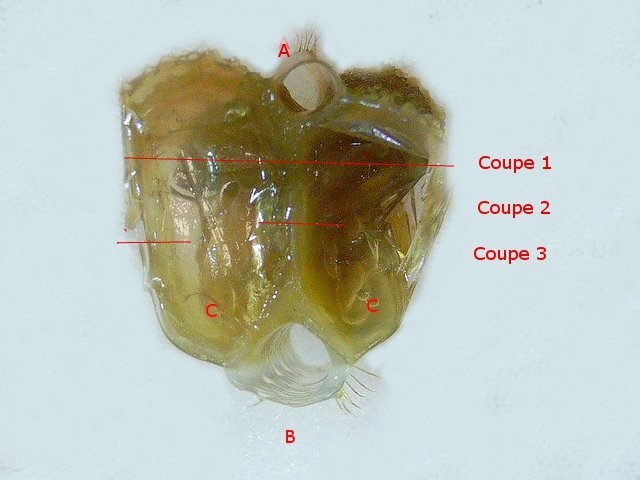
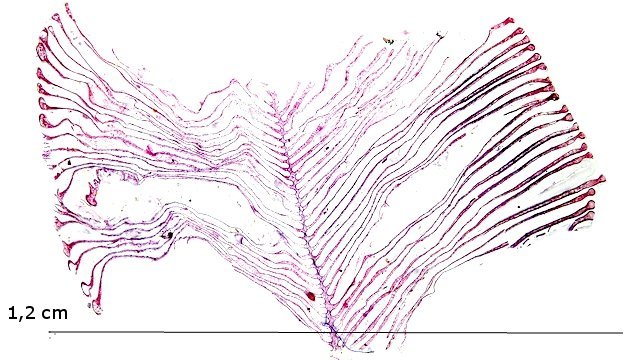
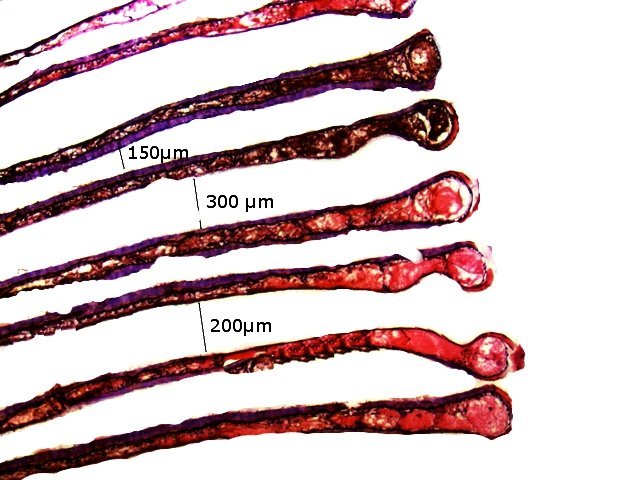
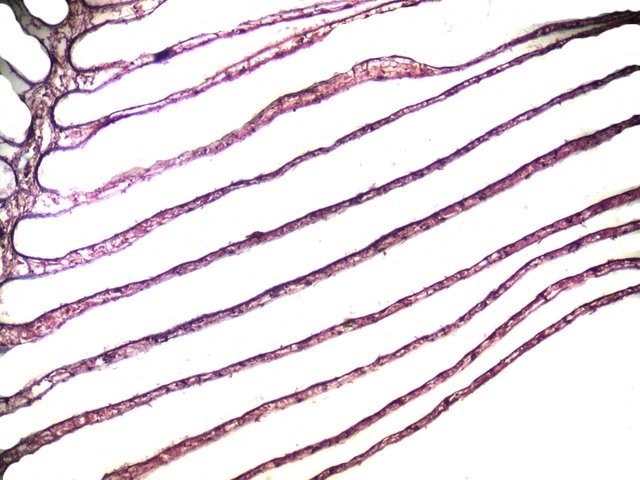
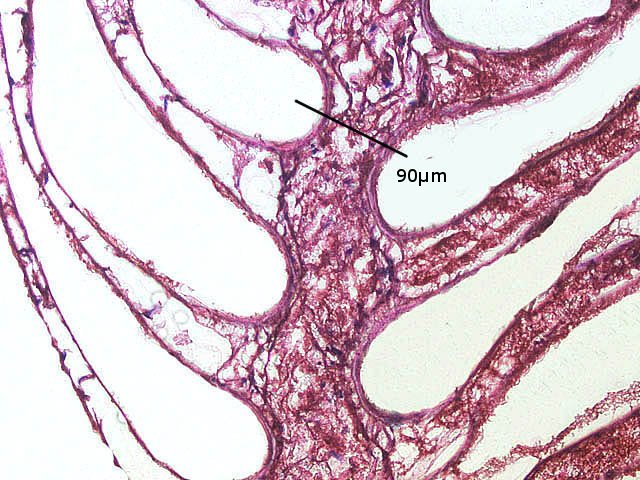
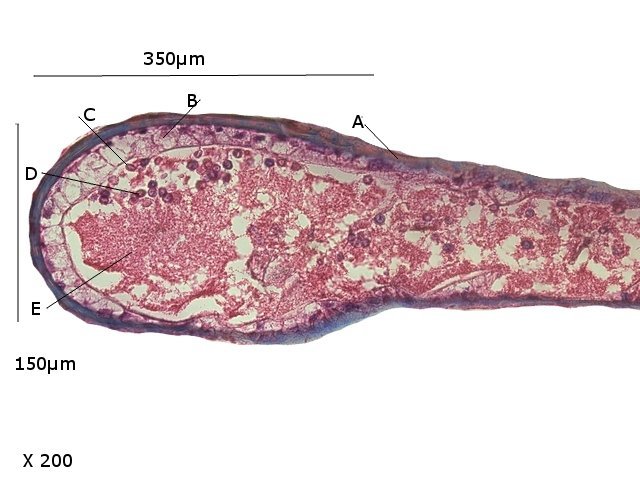
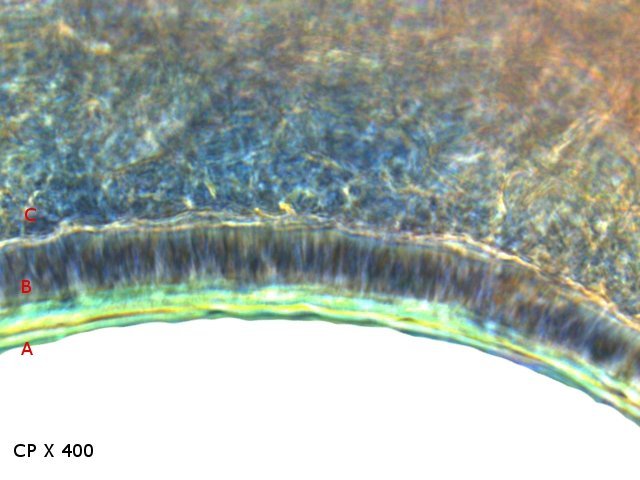
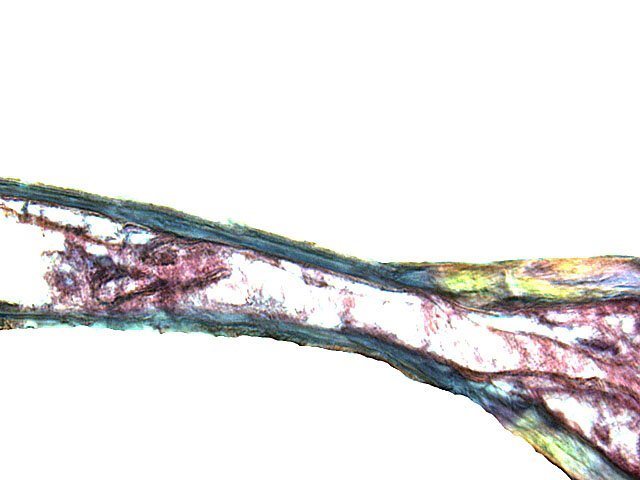
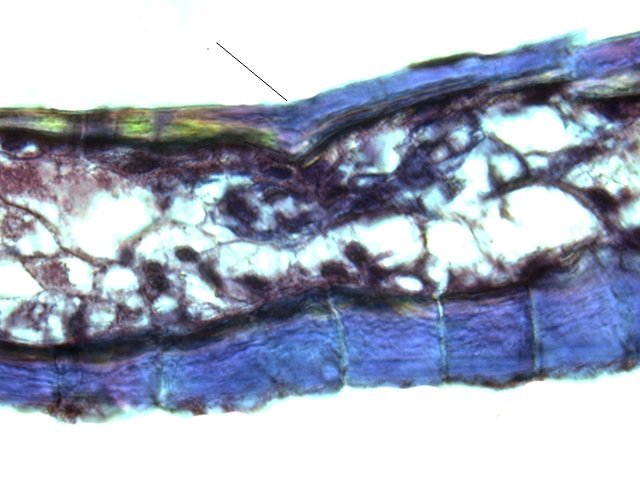
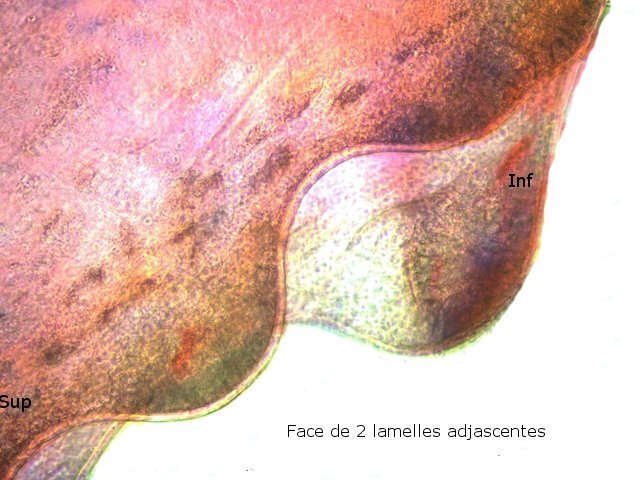
Crabe Branchies Histologie Le premier article nous a fait découvrir l’organisation du massif branchiale et des éléments de ce massif .Il est intéressant de découvrir l’organisation cellulaire de cet organe . Une branchie est organisée par l’assemblage de deux demies lamelles sur un axe médian ;avec la présence d’un vaisseau collecteur sur les deux faces de l’ empilement . Ces colonnes qui forment les branchies sont constituées par l’ entassement d’ une centaine de lamelles –Chaque lamelle est divisée en deux par la présence d’une paroi collectrice de l’ hemolymphe . Coupe suivant le trait 1 ( Coloration trichrome de Masson ): Partie médiane Coupe partie médiane : L’ insertion des deux moitiés de lamelle se fait en alternance. L’ hemolymphe oxygénée au travers de la paroi des lamelles est donc collectée par un canal central qui se vide dans l’hémocœle puis les deux veines périphériques bronchopéricardiaque et leur systéme collecteur. Ce n’est pas un circuit fermé Coupe extrémité distale A Couche de mucus protecteur B Couche faite de cellules pavimenteuses cubiques formant une seule couche cellulaire C Membrane basale D Hemocytes E Protéines coagulées de l ‘hémolymphe La paroi des lamelles Vue de dessus de deux lamelles voisines. Cette paroi est caractérisée par une différence de constitution de la paroi suivant la localisation ( coloration bleu de Toluidine ) En périphérie - donc au contact direct avec le courant d’ eau de mer il existe un épithélium monocouche cubique épais.. Coloration au Bleu de toluidine En utilisant le contraste de phase il est mis en évidence : Par contre dans la partie centrale des lamelles, ce qui représente la majeure partie de la surface d’ échange, la couche cellulaire est faite de cellules très aplaties Elle est organisée en une couche de mucus externe et une membrane basale interne séparant les deux milieux. Cette zone se caractérise par une protection vis-à-vis du flux de l’ eau de mer régnant dans la cavité branchiale c’est-à-dire une circulation plus calme qui va permettre des échanges gazeux tranquilles . Dans ce cas l’espace entre l’eau de mer et l’ hemolymphe est inférieur à 5 µm : la diffusion est donc extrêmement facile. ******************************************************************************************************************* Comment se font les échanges gazeux ? On vient de voir que la paroi des lamelles est d’une très grande finesse puisqu’ elle n’ est faite d’ une couche cellulaire 2. Mécanisme des échanges gazeux L’eau, riche en O₂ dissous, passe entre les lamelles. L’O₂ diffuse passivement (sans dépense d’énergie) à travers cette fine paroi des lamelles, depuis l’eau (où sa concentration est élevée) vers l’ hemolymphe (où sa concentration est plus faible). b. Élimination du dioxyde de carbone (CO₂) L’ hémolymphe arrive aux lamelles chargé en CO₂, produit du métabolisme cellulaire. Le CO₂ diffuse passivement vers l’eau (où sa concentration est plus faible). Une fois dans l’eau, le CO₂ est évacué vers l’extérieur. La diffusion est passive : L’O₂ et le CO₂ traversent la membrane des lamelles branchiales uniquement grâce à un gradiant de concentration (de la zone à haute concentration vers la zone à basse concentration). Pas de réaction chimique : Il n’y a pas de transformation moléculaire de l’O₂ ou du CO₂ lors de leur passage à travers la membrane, donc pas besoin d’enzymes pour catalyser une réaction. Chez les décapodes (crabes, crevettes, homards, etc.), les échanges gazeux se font sans globules rouges ni hémoglobine libre dans le sang (appelé hémolymphe), mais avec des mécanismes biochimiques adaptés à leur physiologie. 1. Transport de l’oxygène (O₂) dans l’hémolymphe a. Pigment respiratoire : l’hémocyanine L hemocyanine est , une protéine respiratoire bleutée (car elle contient du cuivre, et non du fer comme l’hémoglobine) : L’hémocyanine se lie à l’O₂ de manière réversible, selon la pression partielle en O₂ (pO₂). L’hémocyanine est dissoute directement dans l’hémolymphe (elle n’est pas enfermée dans des cellules comme l’hémoglobine). b. Mécanisme de fixation de l’O₂ À haute pO₂ (au niveau des branchies) : L’hémocyanine fixe l’O₂. À basse pO₂ (au niveau des tissus) : L’hémocyanine libère l’O₂. 2. Transport du dioxyde de carbone (CO₂) a. Dissolution directe Une partie du CO₂ est simplement dissout dans l’hémolymphe. b. Formation de bicarbonate (HCO₃⁻) Le CO₂ réagit avec l’eau pour former de l’acide carbonique (H₂CO₃), qui se dissocie en bicarbonate (HCO₃⁻) et protons (H⁺). Pas d’anhydrase carbonique dans l’hémolymphe (:L'anhydrase carbonique est une enzyme qui transforme le CO2 en H2CO3 et inversement). Contrairement aux vertébrés, les décapodes n’ont pas (ou très peu) d’anhydrase carbonique dans leur hémolymphe, donc cette réaction est plus lente et moins efficace. c. Tamponnement L’hémolymphe contient des ions bicarbonate et carbonate qui aident à tamponner le pH, limitant les variations acido-basiques liées au transport du CO₂. 4. Adaptations spécifiques des décapodes La capacité de transport d’O₂ est limitée : L’hémocyanine transporte moins d’O₂ que l’hémoglobine, ce qui limite l’activité métabolique des décapodes par rapport aux vertébrés. Sensibilité à la température et au pH : L’affinité de l’hémocyanine pour l’O₂ est très sensible aux variations de température et de pH, ce qui peut affecter la respiration en cas de stress environnemental. Autres fonctions des branchies Le métabolisme de l’organisme du crabe produit de l’ ammoniaque ou des ions ’ ammonium (NH4+ ) Cette molécule chez le crabe est excrétée au-travers de la paroi des branchies par diffusion passive ( vers l’ eau de mer en raison du gradient osmotique ) Le milieu biologique du crabe est iso osmotique avec l’eau de mer ;- les branchies assurent aussi le maintien de cet équilibre associé au système rénal Ref Invertebrate Zoology Edward E Ruppert – Richard S Fox – Robert D Barnes. Dans la troisième partie nous essayerons de comprendre comment se fait le mouvement de l’ hémolymphe Dominique1 point
-
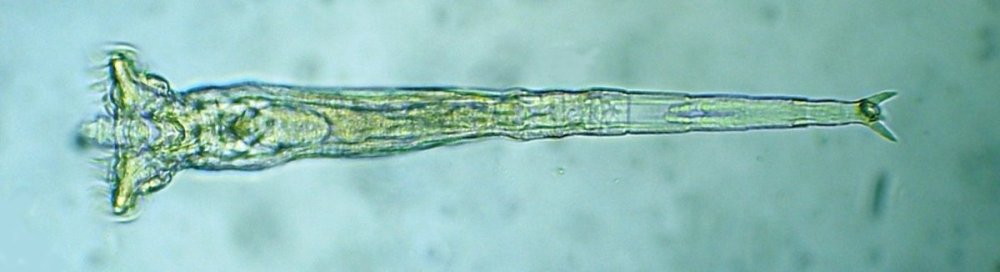
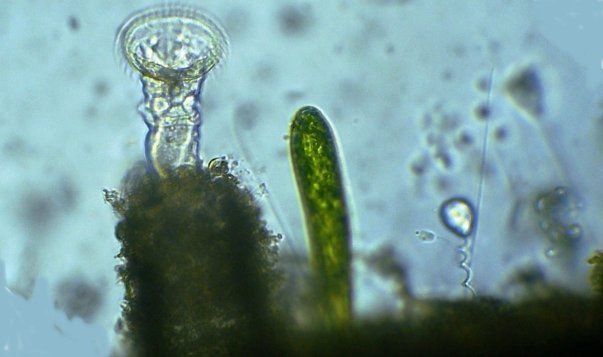
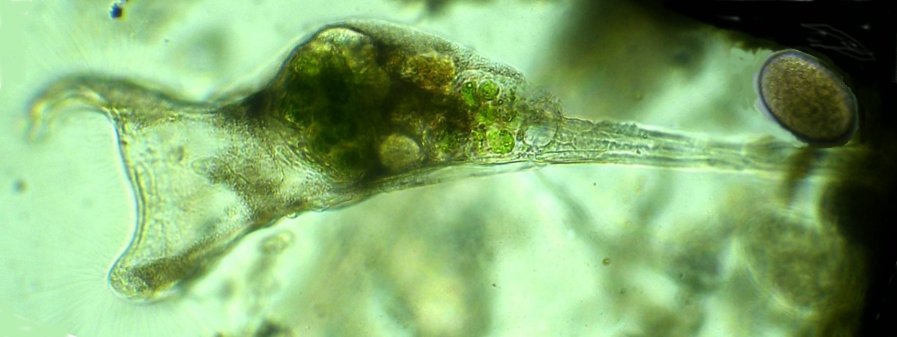
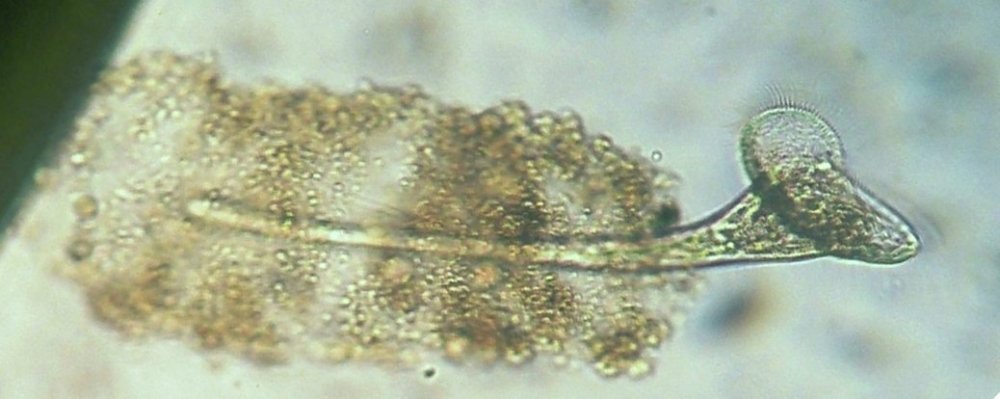
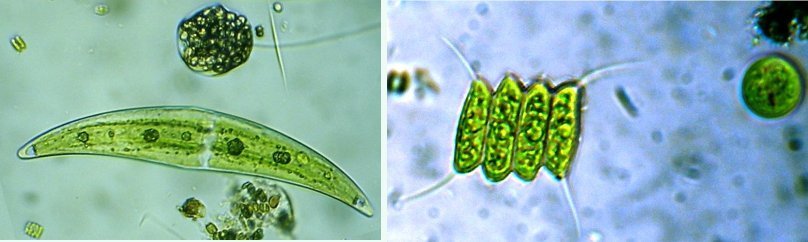
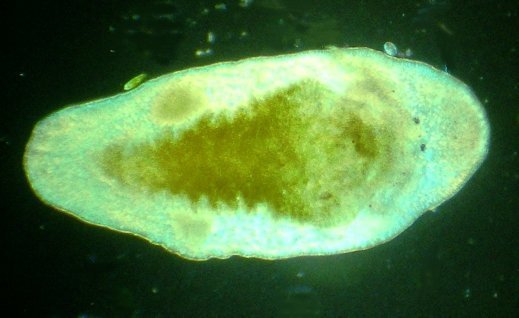
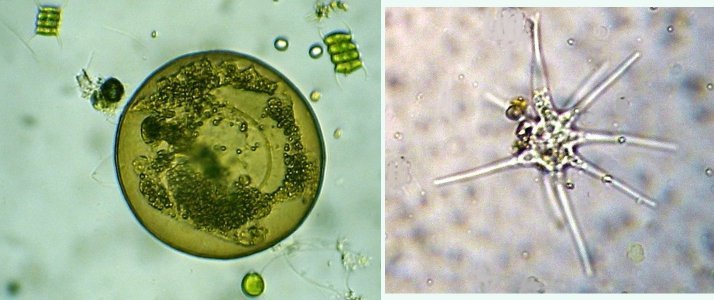
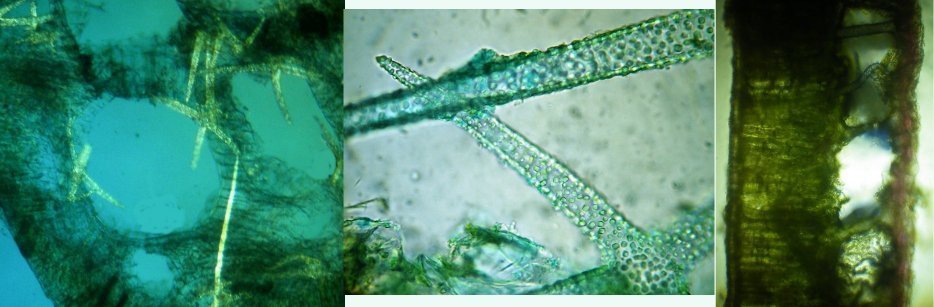
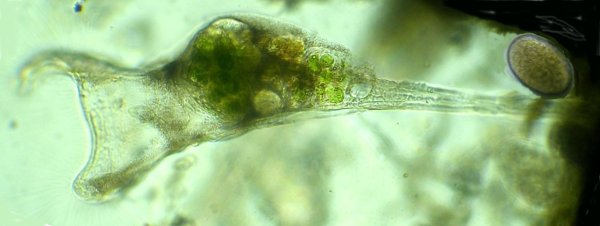
Dans la série "Aventures microscopiques" voici : Les habitants du bassin Souvent nos activités sans rapport avec la microscopie peuvent nous conduire à réaliser des observations aussi inattendues qu’intéressantes. Ce peut être à l’occasion d’un repos dans un parc, d’une après midi de ballade dans la région, une visite dans une jardinerie, ou... une invitation chez des amis qui possèdent un bassin à poissons. C’est ce dernier cas qui va servir à illustrer une exploration des habitants de ce bassin et montrer qu’il n’est pas toujours utile d’aller chercher loin ; j’ai fait ces images rapidement et elles ne sont pas optimisées, mais ce qui importe c’est de voir la variété d’organismes dont chacun pourrait mériter plusieurs heures d’observation . On voit sur cette photo une partie du bassin de 80 cm par 2 mètres et 60 cm de profondeur, garni de nénuphars et de quelques plantes aquatiques. (NB : la sphère en RAKU au premier plan est l’oeuvre de ma compagne, et le bassin appartient à des amis qui nous prêtent leur four à gaz pour ces cuissons raku à l’extérieur de leur maison ) Donc entre deux cuissons , un petit prélèvement de quelques milli litres en grattant les parois du bassin, le dessous des feuilles de nénuphar (en évitant les carpes koï !) est ramené à la maison et voici ce qu’on peut y observer : Un suctoria : avec ses tentacules déployées un rotifère : Un autre rotifére probablement ptygura, qui se construit une logette avec ses boulettes fécales : (on voit aussi une vorticelle contractée sur la droite ) Un autre rotifère plus rare : collothéca avec un œuf : on ne voit pas sur l’image les longs filaments qui lui permettent d’attraper sa nourriture comme avec un filet. Il y en avait plusieurs dans l’échantillon. Un autre protozoaire : stentor qui a produit (ou réutilise?) une logette... à moins que ce ne soit un rotifère ! Des desmidiées ; closterium et scenedesmus Un planaire vu en fond noir : remarquer les taches oculaires à droite une amibe à thèque : arcella à gauche et une amibe libre dans l’eau qui prend cette forme étoilée. Et enfin une vue rapide sur une coupe de tige de nénuphar : à gauche en lumière polarisée on voit bien les lacunes contenant de l’air qui permettent la flottaison ainsi que les sclérites rendues brillantes. Au milieu gros plan sur les sclérites. A droite coupe de la feuille : l ‘épiderme est à gauche de l’image et on voit aussi les lacunes sur la face inférieure qui permettent à la feuille de flotter Il y avait aussi dans l’échantillon quelques euglènes mais pas beaucoup de diatomées… Voici une observation rapide (quand on rentre de la séance RAKU à plus de 100 km de la maison on a quelques autres priorités ! ) ; il ne faut pas garder l’échantillon tel quel plus de 24 heures car beaucoup d’espèces peuvent disparaître ou être mangées par d’autres . On peut dès que possible séparer des spécimens intéressants avec une micropipette et essayer de les cultiver dans un environnement approprié : par exemple prendre suffisamment d’eau du lieu de prélèvement en plus de l’échantillon lui même. En effet dans le cas présent, à 100 km de distance, la composition des eaux locales peut être très différente d’une région à terrains calcaires par rapport à une autre à terrains granitiques.1 point
-
1 point
-
1 point









br.jpg.ccb7a92c200f28d7aa73e9a03c9abe2c.jpg)