-
Compteur de contenus
4 191 -
Inscription
-
Dernière visite
-
Jours gagnés
1
Messages posté(e)s par Jean Marie Cavanihac
-
-
Bonjour
En écrivant les deux articles sur ce thème je me demandais s'il y a des membres qui montent les lames, avec quels types de milieux etc ...
Je sais que Dominique le fait avec ses belles coupes qu'il serait dommage de ne pas conserver... Mais y a t il d'autres amateurs ?
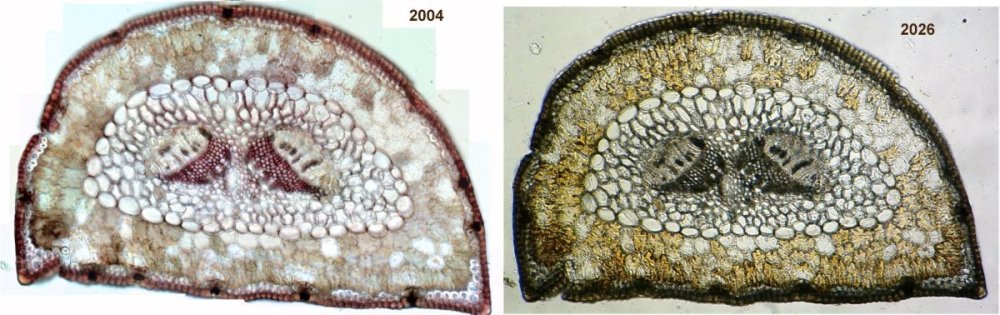
Une image que je n'ai pas mise dans l'article : coupe d'aiguille de pin (la même fraiche et conservée !) à 22 ans d’intervalle
Amitiés
JMC
-
suite de la suite ....
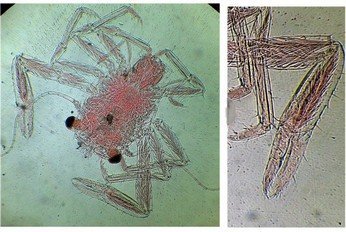
En parlant de spécimens qu on ne rencontre pas souvent (heureusement !) La puce

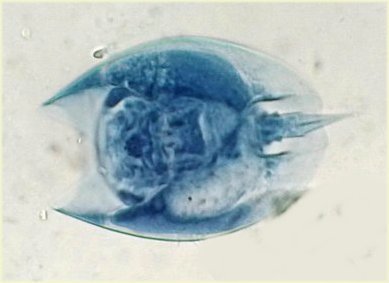
Larve de moustique

Rotifères, : les rotifères avec lorica rigide sont moins déformés. ici : lepadella

Voila quelques exemples de sujets plus ou moins rares . Actuellement je ne fais pratiquement plus de lames , sauf exceptionnellement pour des sujets hyper rares ! La documentation photographique suffit surtout quand , avec l'expérience , on sait a priori les détails qu'il faut observer pour déterminer les espèces ...
-
Il y a quelques temps, j’avais fait une revue de lames réalisées depuis plus de 20 ans.Voir ici :
https://forum.MikrOscOpia.com/topic/20250-revue-de-mes-anciennes-lames/#comment-84293
Les sujets présentés étaient tous d’origine marine et on pourrait se demander si cette technique fonctionne avec des organismes plus – terrestres . La réponse est positive et on va voir que les résultats sont peut être plus faciles à obtenir.
Pourquoi faire des lames montées : simplement pour conserver des spécimens un peu rares ou prélevés dans des lieux où l’on n’a pas souvent l’occasion de revenir. On peut ainsi revoir plus tard des détails qui nous ont échappé lors des observations initiales.
Je rappelle - pour exemple - le protocole utilisé :
- Fixation au picroformol de Bouin
(mais on peut utiliser d’autres fixatifs sans formol) Voir les travaux de Walter Dioni ici : https://www.microscopies.com/DOSSIERS/Magazine/Articles/Walter-Dioni-GALA-1/GALA-1.htm
Le GALA 60 tel que décrit ci dessus fonctionne bien avec les végétaux
- lavage (important : si utilisation du Bouin) retirer l’excédent d’eau
- ajout liquide glycériné qu’on laisse évaporer à l’abri de la poussière
- coloration (si utile) puis nouveau lavage
- montage à la gélatine glycérinée sur platine chauffante
- pose de la lamelle (en évitant de piéger des bulles )
- rinçage lame à l’eau froide pour enlever la gélatine qui a pu déborder de la lamelle
- scellement au vernis à ongle transparent quand la lame est bien sèche
- Ne pas oublier une étiquette d’identification avec le nom du sujet et l’année du montage !
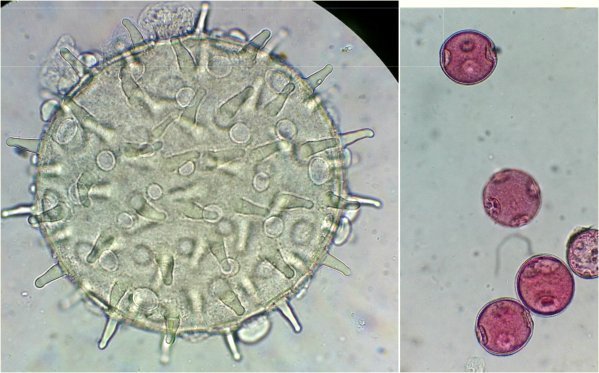
La botanique en particulier se prête bien à la réalisation de ces montages : par exemple les pollens : ici un grain de pollen d’hibiscus (au X 40) et grains colorés d’origine inconnue à droite, on voit bien les pores (NB : penser à noter le nom de l’espèce étudiée sur l’étiquette de la lame : prendre une photo de la plante si besoin). Parfois il est utile de dégraisser le pollen dans une goutte d’alcool éthylique avant de procéder au montage

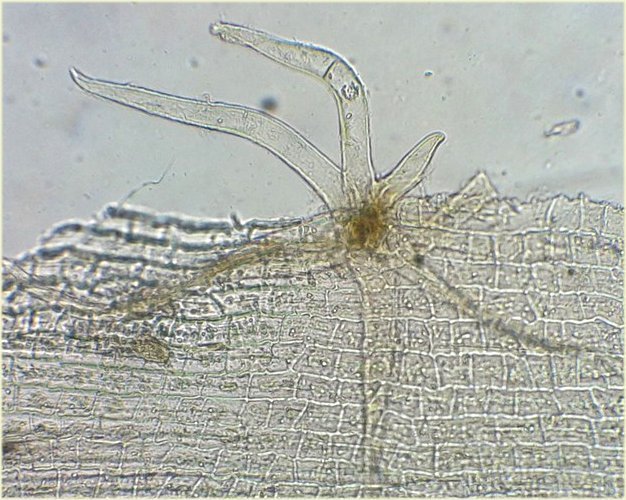
Poil de tige de lierre :
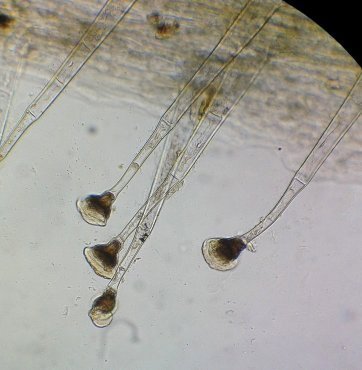
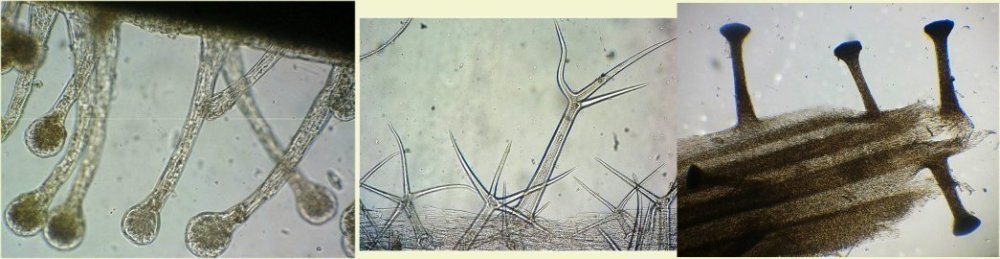
Poils de tiges de géranium : leur extrémité en forme de coupe porte encore une goutte d huile odorante

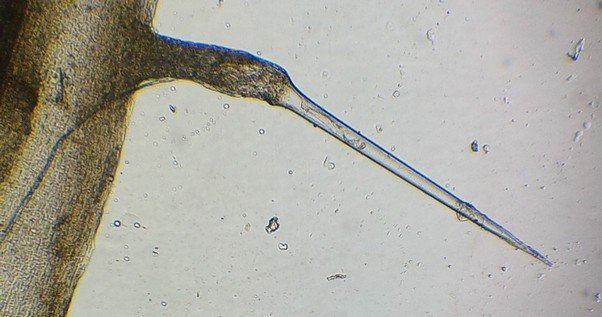
Poil d'ortie : le poil est creux et lorsque la point se brise , la substance irritante contenue dans la base est injectée
Divers poils ( je n'ai pas suivi mes conseil et pas identifié leur provenance !! )
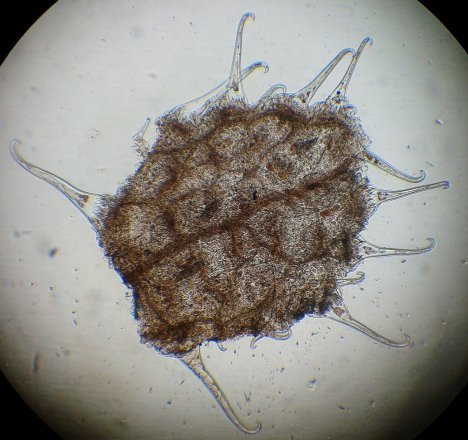
Mais il y a aussi des graines qui utilisent des poils pour se disséminer par exemple en s’accrochant à la fourrure des animaux (ou à nos vêtements !) . C’est ce genre d’observation qui a conduit à l'invention du Velcro . Image au x 2,5

Un peu plus technique : les coupes végétales , tiges, bourgeons etc . L’habileté du botaniste intervient d’avantage mais quelques accessoires simples et peu coûteux permettent d’obtenir des résultats intéressants par exemple :
On peut rencontrer des bulles piégées dans le parenchyme. On peut les atténuer en trempant la coupe dans un agent mouillant par exemple UNE goutte de liquide vaisselle dans un demi verre d ‘eau puis dans un mélange 50/50 eau alcool.
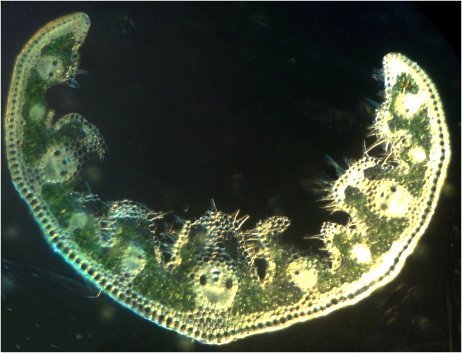
Un classique des livres de SVT : la coupe de feuille d’oyat qui illustre l’adaptabilité en milieu sec : la feuille se referme sur elle même pour réduire la surface exposée : X 2,5 fond noir :

Coupe d’une aiguille de pin (plus facile à trouver que les oyats) Ici la même à l’état frais: https://forum.MikrOscOpia.com/topic/5596-coupe-daiguille-de-pin/#comment-2236

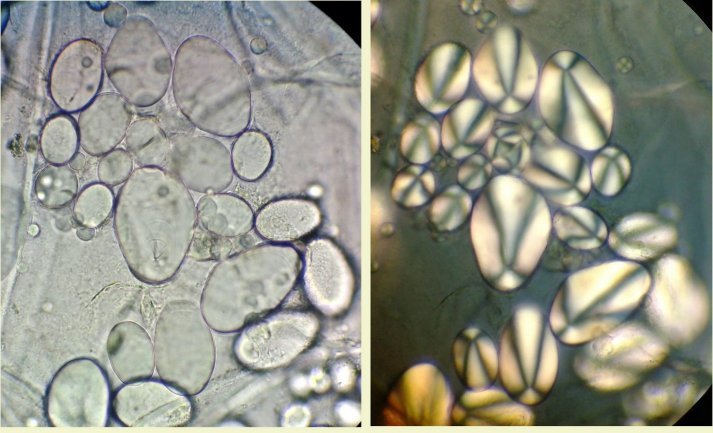
Divers botanique : amidon de la banane (en fond clair et polarisation),

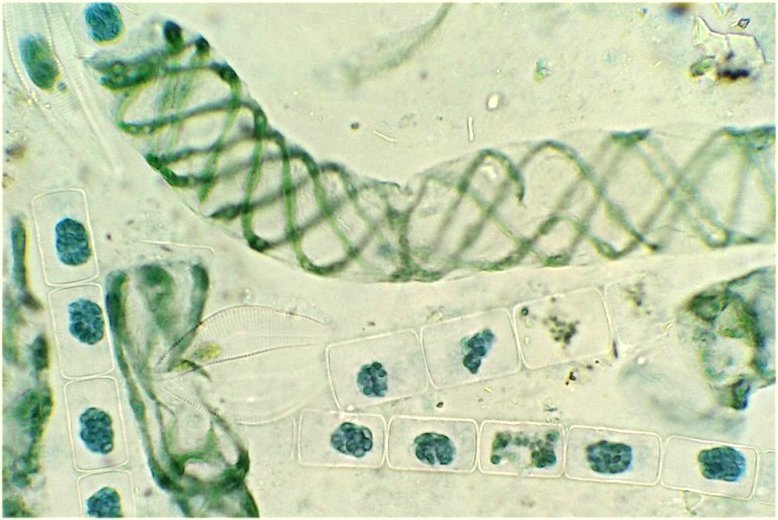
Algues d’eau douce (mais se distordent lors du chauffage) ici spirogyres

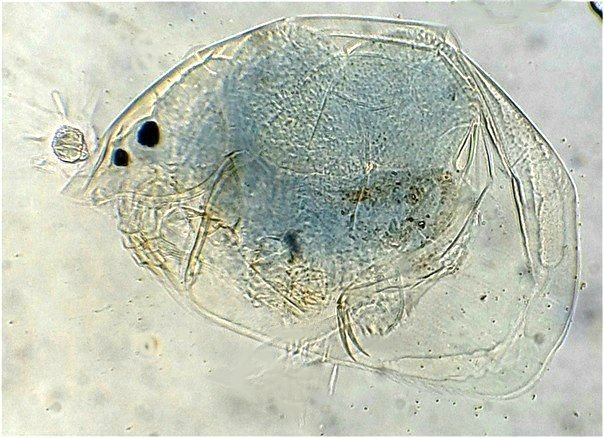
Mais il est aussi possible de conserver des formes animales : Cladocère d’eau douce (probablement Chydorus)

Insectes :cornée d'un oeuil de papillon, une écaille des ailles de papillon

Un insecte (piqueur !) entier : taille 1 mm (composition de 4 images par Image Composite Editor). Peut etre Scleroderma Domesticum rendu transparent par bain de soude

Une larve de chiromonidé colorée à l'éosine , qui avec le temps, est restée fixée sur les muscles :
-
Bonjour
Avec la météo actuelle entre la pluie et le vent qui ne favorisent pas les sorties, pourquoi ne pas revoir des lames anciennes que nous avons faites il y a 10, 20 ans voire plus ?
Je vous propose cet article qui démontre plusieurs choses : le montage à la gélatine glycérinée ou glycérine gélatinée bien que modeste milieu de montage ne se comporte pas trop mal. J'avoue quelques erreurs : trop ou pas assez de milieu sur la lame (le bon dosage vient avec l'expérience !) , mauvaise étanchéïté... etc
Hommage à notre ami Walter qui a beaucoup expérimenté en ce domaine , et dont j'invite à lire les articles sur les milieux de montage
Pour vous permettre de jouer un peu , deux références bibliographiques à des romans littéraires se sont glissées dans le texte (une est plus difficile)... Retrouverez vous leurs auteurs ?
Amitiés
JMC
-
J’aurais pu intituler cet article « Vingt ans après » mais le titre est déjà pris Le but est de revoir - au moins 20 ans après leur réalisation -, diverses lames que j’ai montées selon le protocole suivant :
- Fixation au picroformol de Bouin
- lavage
- ajout liquide glycériné laisser évaporer ou enlever le surplus par le coin d’un mouchoir papier
- coloration (si utile) puis lavage
- montage à la gélatine glycérinée ** (faite maison) sur platine chauffante
- pose lamelle
- rinçage lame à l’eau froide pour enlever la gélatine qui a débordé de la lamelle
- scellement au vernis à ongle quand la lame est sèche
Au début de mes observations, surtout de plancton, je souhaitais garder les sujets pour examen ultérieur, quand j’aurais eu plus de documentation sur leurs caractères spécifiques. La photo est un bon moyen, mais souvent les éléments d’identification fine n’y sont pas toujours visibles selon comment a été faite la mise au point lors de la prise de vue.
Pour des sujets très transparents (et sachant qu’ils s’éclaircissent avec le temps ) j’utilisais deux colorants : l’éosine et le vert de bromocrésol ( un indicateur de pH virant bleu à pH=4)
Rangement dans des boites faites maison avec du carton ondulé (5 boites comme celle ci ) ce qui fait dans les 250 lames à explorer.
Noter la petite astuce consistant à repérer sur l’étiquette la position approximative du sujet sous la lamelle (surtout s’il y en a qu’un ) : point marqué par la flèche rouge.

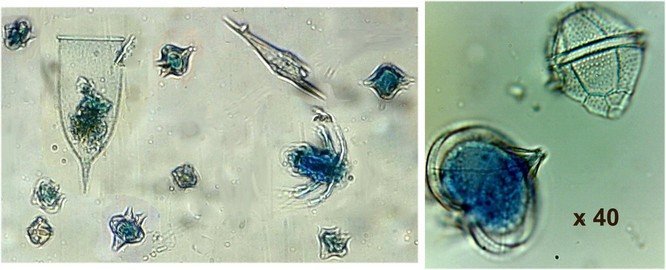
Bien entendu après plus de 20 ans les lames ne sont pas toutes en parfait état ! Les principaux défauts : rétraction de la gélatine qui n’englobe plus le sujet (récupérable, on le verra), développement de structures qui ne semblent pas être des moisissures (peut être des bulles ?), sujets non colorés devenus trop transparents …Par exemple cette anémone de mer encore visible mais entourée de ces structures

Comment rajouter de la gélatine ? C’est assez facile avec la platine chauffante ci dessous (alimentée par le transformateur de la lampe du microscope). A gauche exemple de gélatine rétractée (flèches) sur une lame contenant un polype de méduse

On gratte le vernis sur un coté de la lamelle au plus prés de la bulle, on pose la lame sur la platine et on ajoute un fragment de gélatine sur la partie grattée : celle ci en fondant s’infiltre par capillarité et on peut éliminer les bulles en tapotant légèrement sur la lamelle .

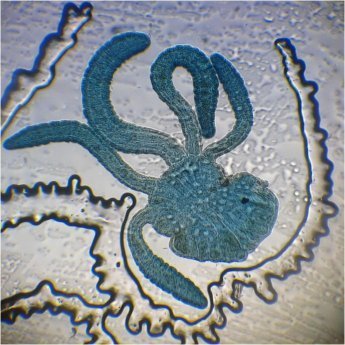
Voici un effet non prévu du fixateur : le Bouin est acide (contient de l’acide picrique) et ramollit voire dissous les structures contenant du calcaire, d’où l’allure « mole » de cette larve d’ophiure (a droite spécimen vivant) .Donc attention !

Voyons les résultats sur divers sujets planctoniques et ce qu’ apporte l’examen à postériori de ces lames pour retrouver des détails qui ont échappé aux premières observations
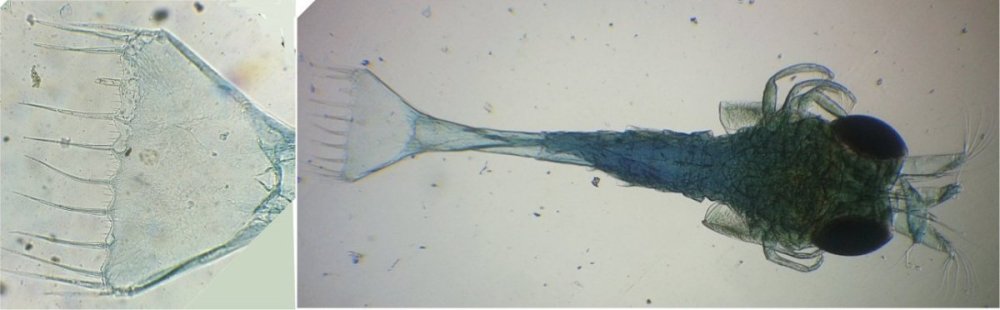
Voici une larve de galathéa. (espèce de crabe) l’observation des détails de la queue permet de préciser l’espèce
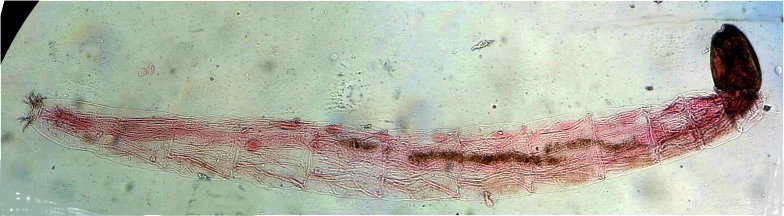
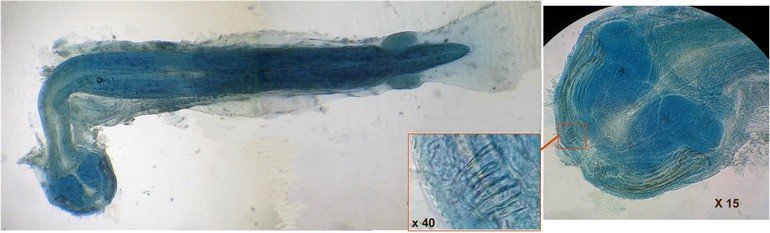
Autre exemple : sur ce chaetognathe Sagitta : on voit très bien sur la tête les crochets de chitine mais la littérature fait état de dents antérieures et postérieures, dents antérieures que je n’avais pas vu et que l’on va retrouver dans le détail au X 40

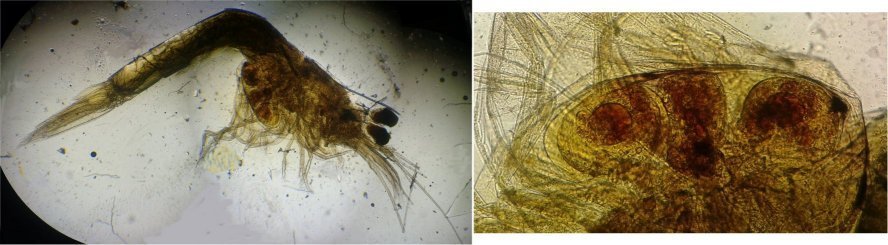
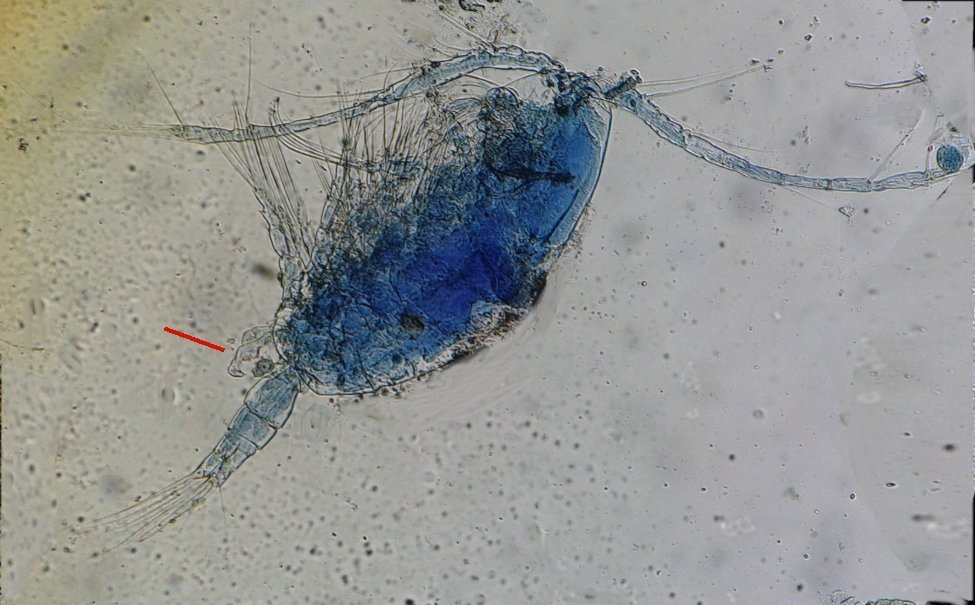
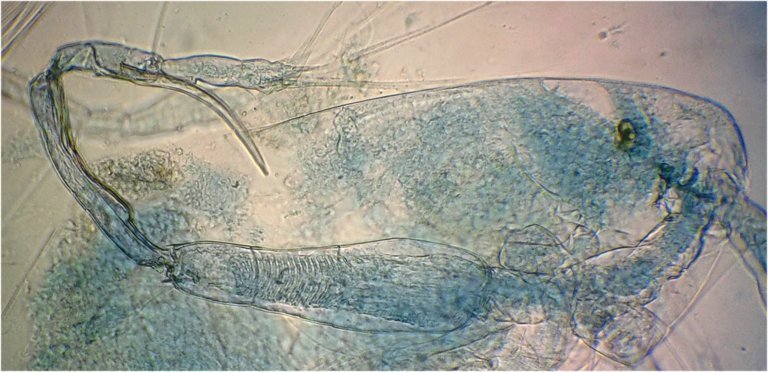
Autre exemple encore plus intéressant de recherche à posteriori: j’avais remarqué sur cette femelle copépode ( calanus paracartia identifié à postériori sur cette lame ) un détail qui m’avait échappé : flèche rouge avec détail à droite : coloré en rose (sur l'image) on voit un spermatophore
Lors de l’accouplement le mâle maintient la femelle grâce à une patte modifiée en pince et lui transfère le spermatophore qui va adhérer à l’abdomen de la femelle comme spermathèque et les spermatozoïdes contenus féconderont ses œufs en temps utile …voir ici les détails :
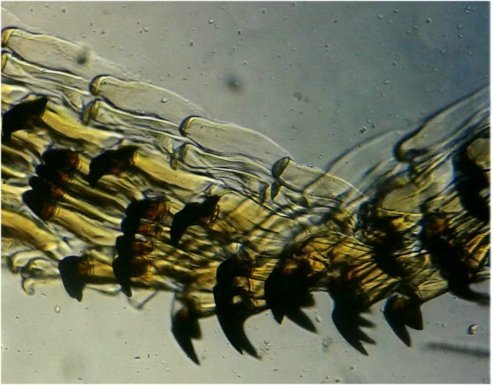
Autre sujet facile à conserver : radula de patelle ;La patelle, coquillage qui a la forme d"un chapeau chinois, possède (comme les escargots) cet organe chitineux qui lui permet de râper les algues

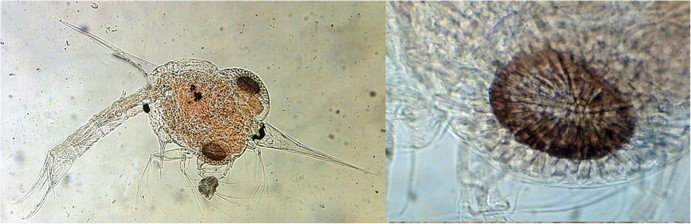
Sur cette larve de crabe stade zoéa , le X 40 sur l’œil permet de voir les ommatidies

A la longue les colorations à l’éosine, qui étaient uniformes, se différencient en se fixant sur les muscles ; par exemple sur ces gnathopodes de caprelles : peut être à cause d’un rinçage insuffisant du Bouin car l’éosine se décolore en milieu acide

Idem pour cette larve de crabe stade mégalops : les fins muscles sont colorés en rose

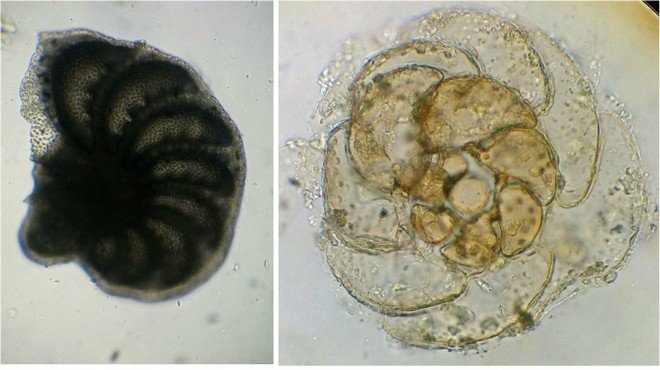
Avec le temps : le foraminifère de droite a perdu la matière minérale (acidité du Bouin sur le calcaire ? ) et on voit l’organisation des chambres , alors que l’autre est resté inchangé et peu transparent.

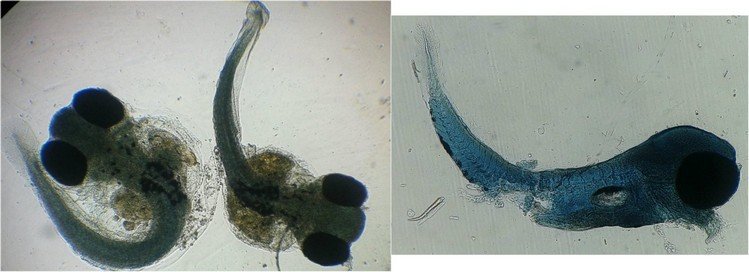
Autre exemple de bonne conservation : ces alevins de poisson , sur celui de droite : on voit la vessie natatoire et les vertèbres (X 2,5)

Bonne conservation pour ces vers : polychaete qui a beaucoup pâli à gauche et annelide

Un dernier exemple avec ces dinoflagellées et ce tintinide Favella

Voilà donc quelques exemples de montages à la gélatine sur des organismes marins. Je ne sais pas si les résultats seraient meilleurs avec le Baume du Canada, ou les résines synthétiques modernes. Je crains que les déshydratations préliminaires ne déforment beaucoup les échantillons. Un avantage de la gélatine est sa rapidité d’utilisation. Le procédé fonctionne bien avec les plantes et les coupes végétales. Mais ceci est une autre histoire ….
* Note : une recette de gélatine de notre regretté Walter Dioni et d’autres milieux de montage
https://www.microscopies.com/DOSSIERS/Magazine/Articles/WD-MILIEUX/Montage.html
-
Bonjour Daniel
En cette saison voir plutôt le rayon plantes d'intérieur plus abrité du froid . Autre points de prélèvement (hors jardinerie) : les dépôts verts sur fontaines et vasques à l'extérieur... Il n' y a pas forcément beaucoup de choses qui bougent mais on trouve des diatomées, desmidiées etc...toute l'année.
Bonne idée que la journée d'animation : cela pourrait faire l'objet d'un mini reportage dans le forum !
Amitiés
JMC
-
Bonjour Daniel
Merci de lire aussi ma prose en Anglais ! (ça m'oblige à faire des efforts supplémentaires de rédaction, c'est bon pour le cerveau !)
J' avais déjà parlé de cette observation dans notre forum. En fait j 'ai été un peu lapidaire sur la raison de ne pas mettre de lamelle : c'est surtout pour pouvoir accéder à un sujet intéressant (avec une micropipette) parmi les divers débris que l'on trouve sur la lame , pour le transférer ailleurs (lame propre ou récipient de culture) Un spécimen sous lamelle n'est quasiment pas récupérable (quoique *)
* petite astuce : rajouter de l'eau sur le bord de la lamelle pour qu'elle commence à flotter puis la déplacer avec précaution pour que le spécimen sorte dans la goutte hors de la lamelle puis vider cette goutte dans le nouveau récipient en ajoutant si besoin de l'eau pour bien rincer la lame. Si la lamelle tombe dans le récipient, on la récupèrera plus tard...
Amitiés
JMC
-
Bonjour Dominique
Bonne question ! Les copépodes sont ubiquistes; on les trouve dans tous les milieux aquatiques voire des flaques d'eau, eaux saumâtres etc . Il n'y a pas de différences morphologiques entre espèce marine et eau douce.
Dans mes observations j'ai trouvé des cyclopoïdes (le plus commun étant le cyclops) dans l'eau douce et aussi en eau de mer, mais pas de calanoïdes ni harpaticoïdes dans l'eau douce (encore que je n'ai pas beaucoup de choix pour les sites en eau douce !) . Je pense que la densité des espèces est beaucoup plus grande en eau de mer ce qui facilite la capture en nombre. Ce qui m'a étonné c'est de rencontrer Tigriopus qui n'est pas référencé en Méditerranée .
Merci pour ton appréciation sur la dernière image "live" (: on voit le flou des maxillipédes qui s'agitent) , mais il faut être rapide pour la prise de vue. !
Amitiés
JMC
-
Suite ...
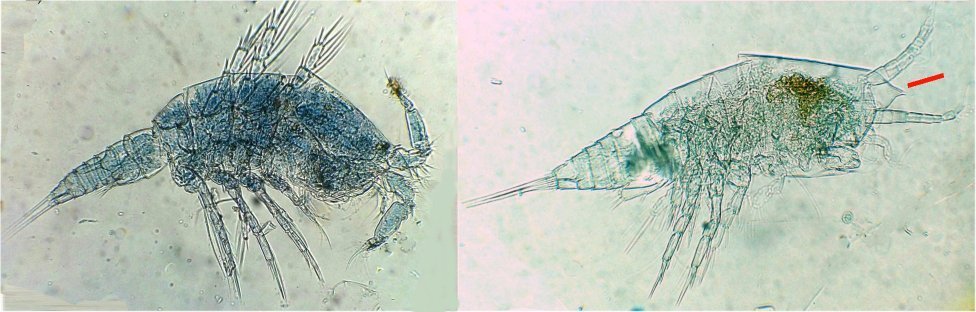
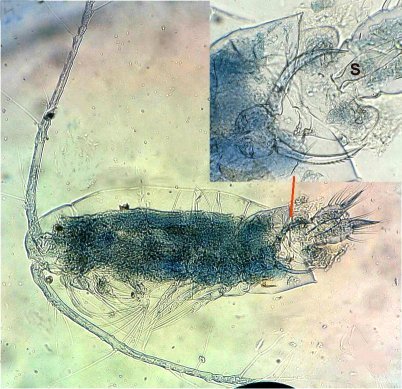
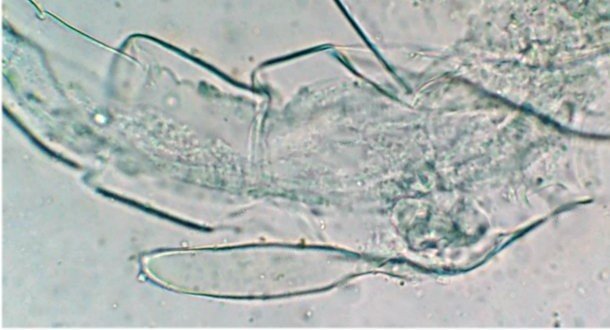
Quatrième espèce : cette fois ordre des Harpaticoïdes : euterpina acufrontis : deux antennules courtes géniculées* sur le mâle à droite , rostre* bien visible sur la femelle

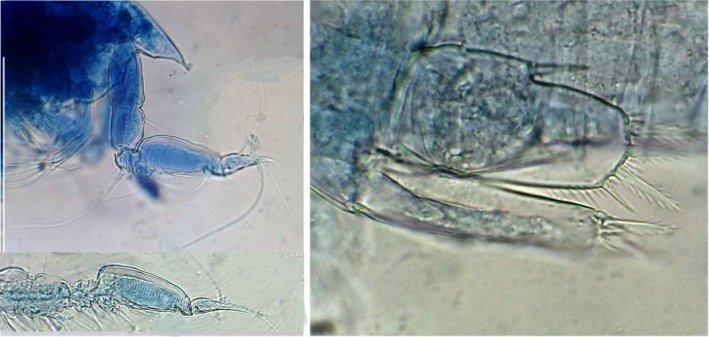
mage de gauche détail d’une antennule mâle pliée et étendue et image à droite : P5 de la femelle très semblable à celle du mâle.

Sur ce spécimen mâle on distingue un spermatophore* qui n’a pas encore été transféré sur la femelle détail au x 40

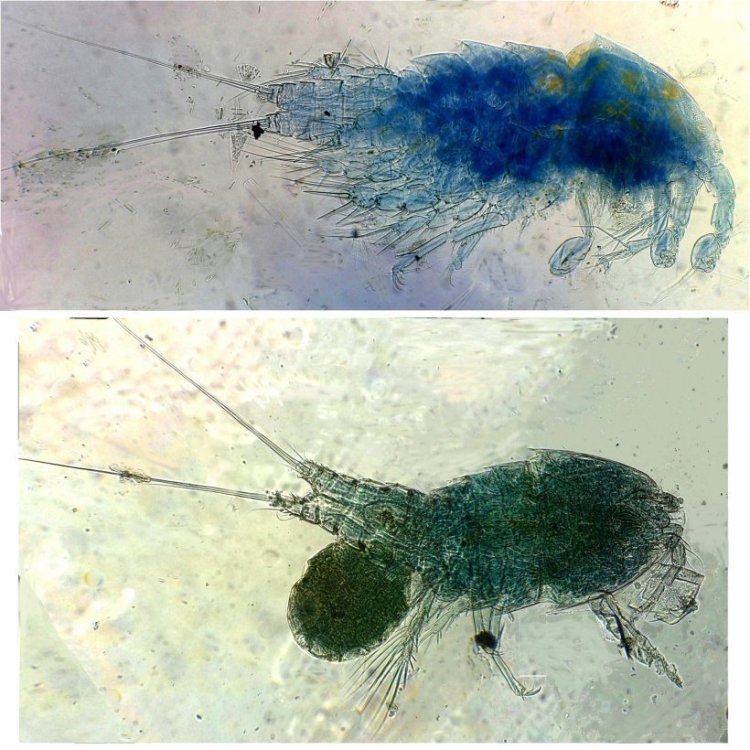
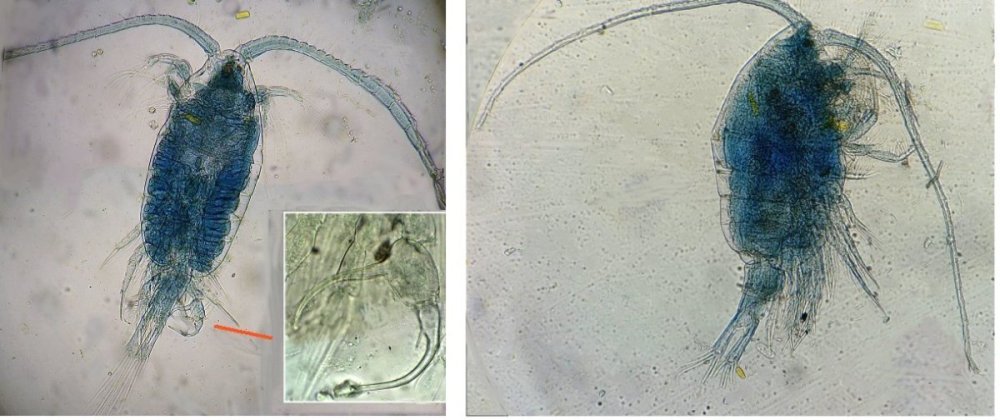
Cinquième espèce : harpaticoïde qui m’ a été difficile à identifier : Tigriopus. (Tig pods) Il en existe une quinzaine d’espèces. Leur couleur jaune est due à un pigment orange (astaxanthine) qui est synthétisé pour les protéger des rayons UVA et UVB du soleil, car les zones à faible profondeur (flaques) où ils vivent sont soumises aux rayons solaires.
Les antennules, qui possèdent des détecteurs chimiques, permettent au mâle de reconnaître les propriétés chimiques d’une femelle en période de reproduction.
On remarque les antennules du mâle de forme très caractéristique qui aident à l’accouplement et aussi la présence de maxillipèdes* chez les deux sexes.
On voit bien le sac ovigène chez la femelle .
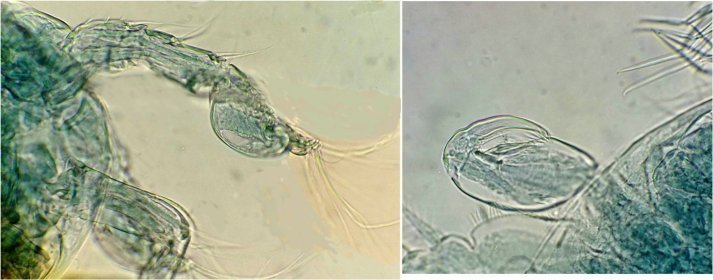
Détail des antennules du mâle image de gauche (on y distingue des poils sensitifs ) et à droite un des deux maxillipèdes objectif x 40

Il semble que cette espèce soit plus rare en Méditerranée : je ne l’ai pas trouvée dans « Faune de France biblio Ref 3 ni sur Ref 4 (base de donnée française importante )» mais seulement chez « G.O. Sars – Ref2 ».
L ‘espèce est sensée se trouver sur la cote Ouest de l’Europe mais ces spécimens ont bien été recueillis en Méditerranée !
Lexique :
Antennule : Le plus antérieur des appendices pairs des crustacés, formé d'une base contenant un statocyste et de deux fouets, aux fonctions tactiles.
L'une des fonctions de l'antennule est la détection de la nourriture, des mouvements de l'eau, des prédateurs
Géniculée : avec une articulation rappelant celle du genou
Spermatophore : une capsule contenant des spermatozoïdes créée par les mâles de diverses espèces , et transférée dans ou a proximité de l'ovipore de la femelle pendant l’accouplement
Ovipore : organe sexuel femelle en forme de pore qui est inséminé par le spermatophore déposé par le mâle
Maxillipède : Le maxillipède (littéralement « pied-mâchoire ») est un appendice du péréion (ou thorax) modifié chez certains crustacés et impliqué dans la nutrition. Le maxillipède est une sorte de « patte » thoracique qui a été transformée et qui sert à la mastication .
Rostre : Prolongement pointu, vers l'avant du corps chez les insectes et crustacés
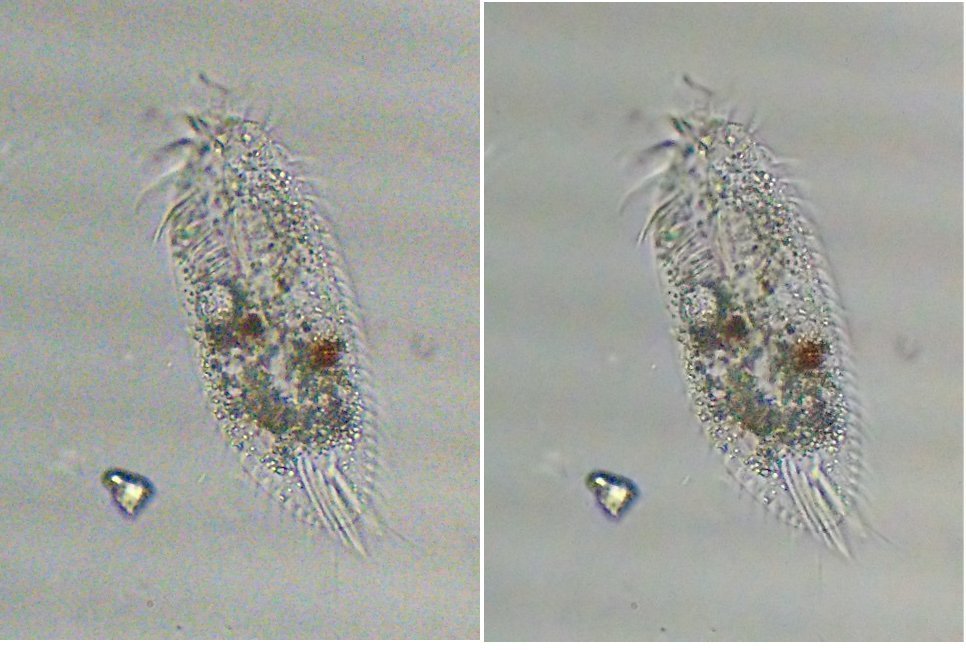
Pour terminer et montrer la beauté d’un copépode vivant voici une image en fond noir pour s’exercer à la détermination : quel ordre, mâle ou femelle, espèce ?? Les indices sont ci dessus !
JMC
-
Les copépodes, sont de petits crustacés, qui constituent une grande partie du zooplancton ; ils représentent 12000 espèces où l’on distingue 10 ordres .
Dans les prélèvements au filet à plancton (ici maille de 200 µm), le nombre de copépodes recueillis est très important en particulier les mois d’été. En prenant quelques précautions : conservation au frais de l’échantillon et observation rapide (entre 2 et 3 heures après prélèvement), de nombreux spécimens peuvent être observés vivants.
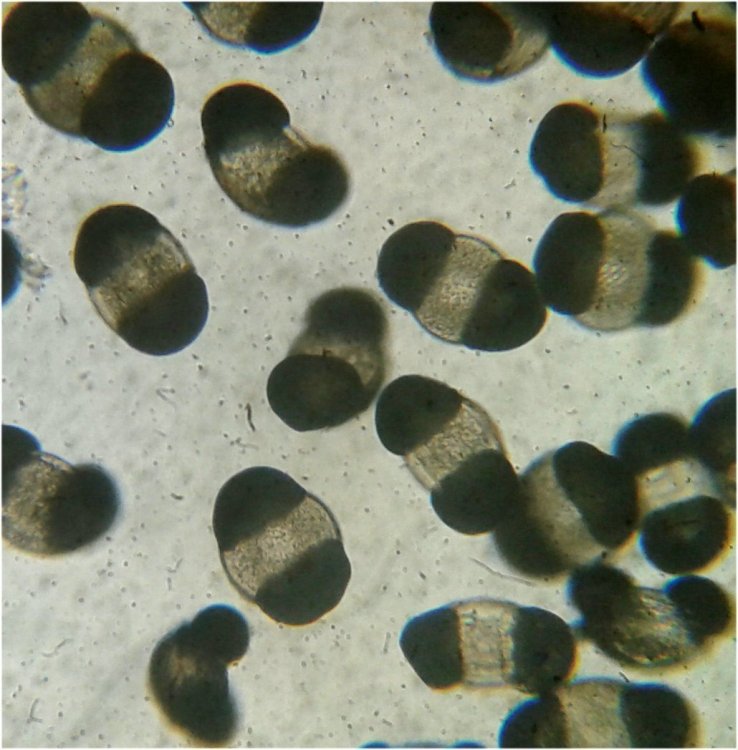
Cependant en raison de leur nombre élevé, la concentration en oxygène baisse rapidement dans le flacon et vient ralentir leurs mouvements : il tombent au fond en constituant une « soupe » de copépodes et le prélèvement d’une seule goutte de ce dépôt ramène plus d’une dizaine de spécimens sur la lame. Dans l’image ci dessous , il faut donc diluer ! Ce grand nombre de spécimens va permettre de les figer en diverses positions et sur la quantité présente on peut trouver le mâle et la femelle .

Pour les conserver : fixation au picroformol de Bouin directement sur lame, coloration par le vert de bromocrésol (pas vraiment un colorant mais un indicateur de pH) et montage à la gélatine glycérinée. J’ai ainsi réalisé plusieurs lames sur plusieurs années successives . Ceci fait je remets les reste du flacon à l’eau pour nourrir les alevins de poissons ...
J’ai un peu négligé de m’intéresser plus tôt aux copépodes car je recherchais des sujets plus rares. En reprenant 6 ou 7 lames, dont certaines datent de 20 ans, j’ai pu identifier plusieurs espèces homogènes en quantité dans les échantillons.
Voici quelques définitions de la morphologie des copépodes qui vont être utiles pour la suite :
de plus , dans le texte, les mots repérés par « * » renvoient au lexique en fin d’article

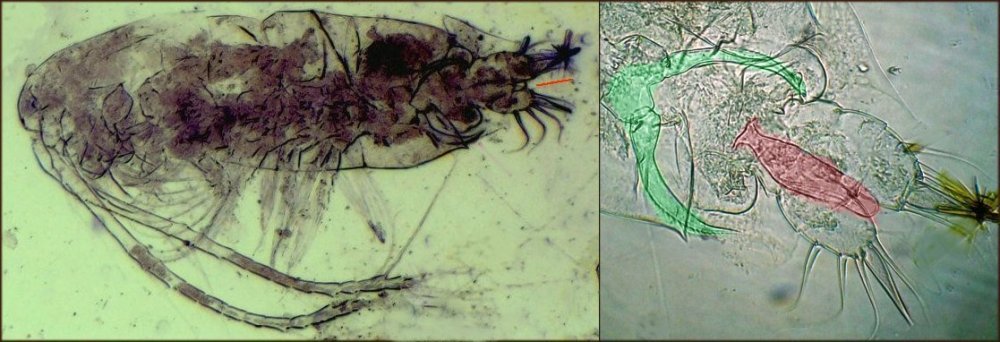
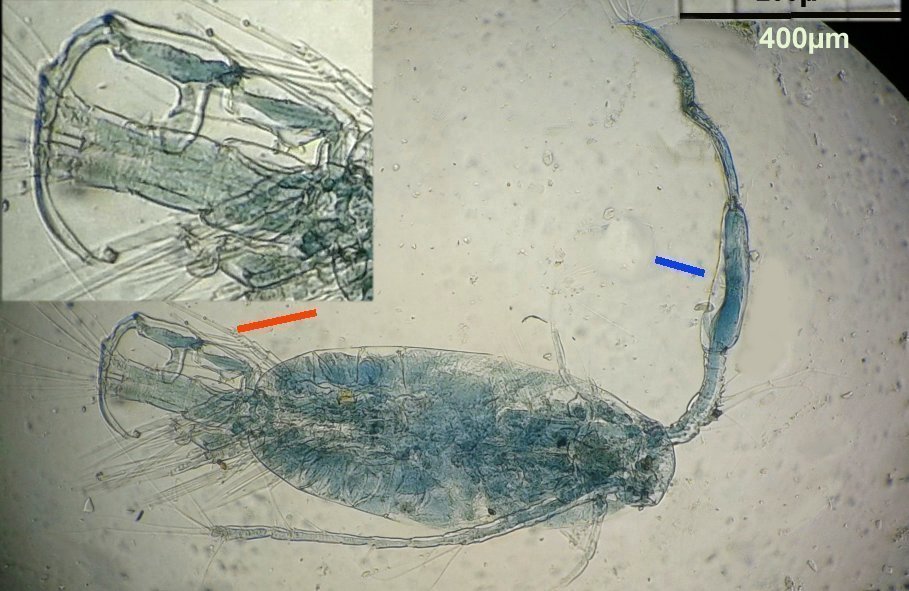
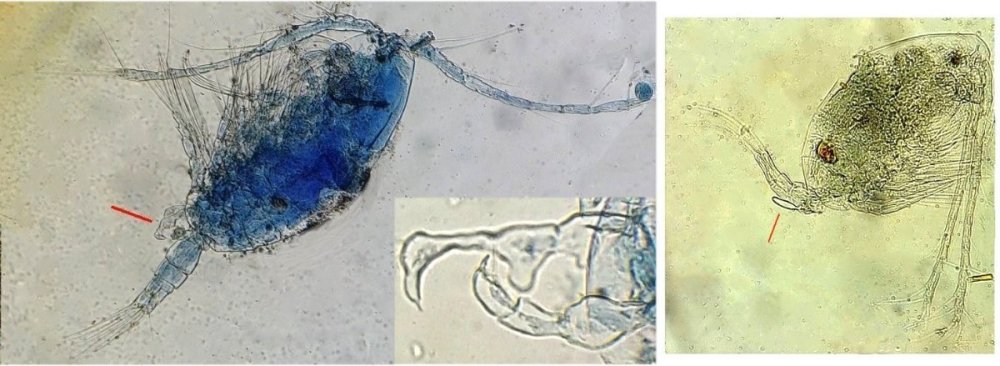
L’une des lames observées montrait un spécimen de l’ordre des calanoïdes, reconnaissables à leurs longues antennules* ; dont une des pattes de la dernière paire (P5) était largement modifiée en forme de pince : Ce dimorphisme sexuel est adapté à leur reproduction.

La flèche rouge montre P5 modifiée et la flèche bleue une autre caractéristique du spécimen mâle : la présence d’une antennule géniculée* utilisée dans l’accouplement.
La femelle ne possède pas d’antennule modifiée, les 2 sont identiques . P5 en forme de pince différente de celle du mâle :voici la femelle et la pince en détail : (S : spermatophore * )

Il est recommandé de lire ces liens pour voir plus en détail les modalités d’accouplement.
https://forum.MikrOscOpia.com/topic/20116-copépode-calanus-arcatia-arcaturia-clausi/#comment-83460
Les deux autres spécimens ci dessous sont de l espèce acartia grani (Male à gauche et femelle à droite). La pince du male est similaire à celle de pacartia grani mais semble moins sophistiquée. (détail à l’ objectif x40)
La femelle n’a pas de pince à la différence de celle de paracartia
on voit sur l’image à droite le spermatophore * collé sur l ‘ urosome de la femelle (flèche rouge) avec détail ci dessous à l’objectif x 40

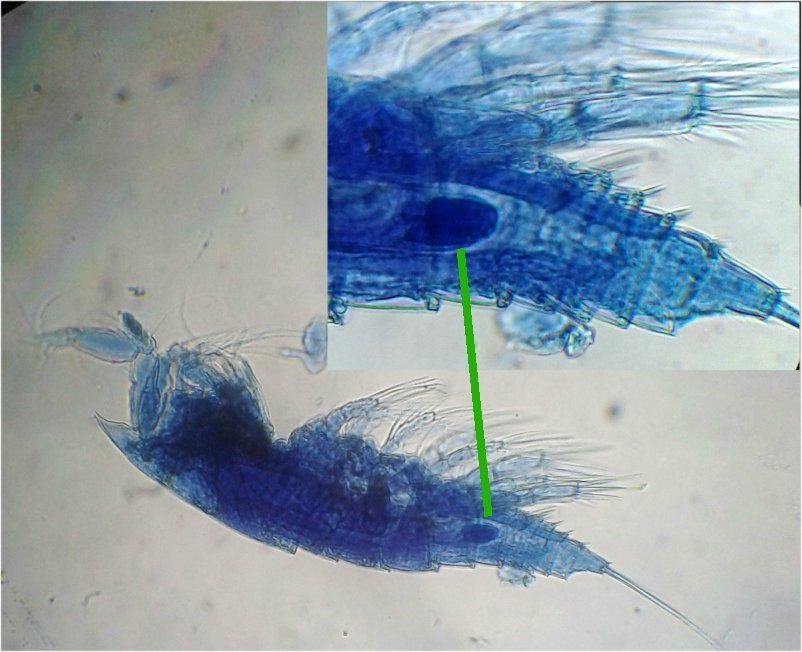
Troisième espèce : Centropages ordre des calanoïdes aussi . La pince du male (photo de droite) est plus fine. On remarque aussi l’antennule géniculée * sur la droite du mâle
une épine asymétrique sur la femelle (flèche bleue) orienterait vers centropages hamatu ; noter l’ovipore * (flèche verte)

-
suite
des ailles
des enveloppes céphaliques / pièces buccales
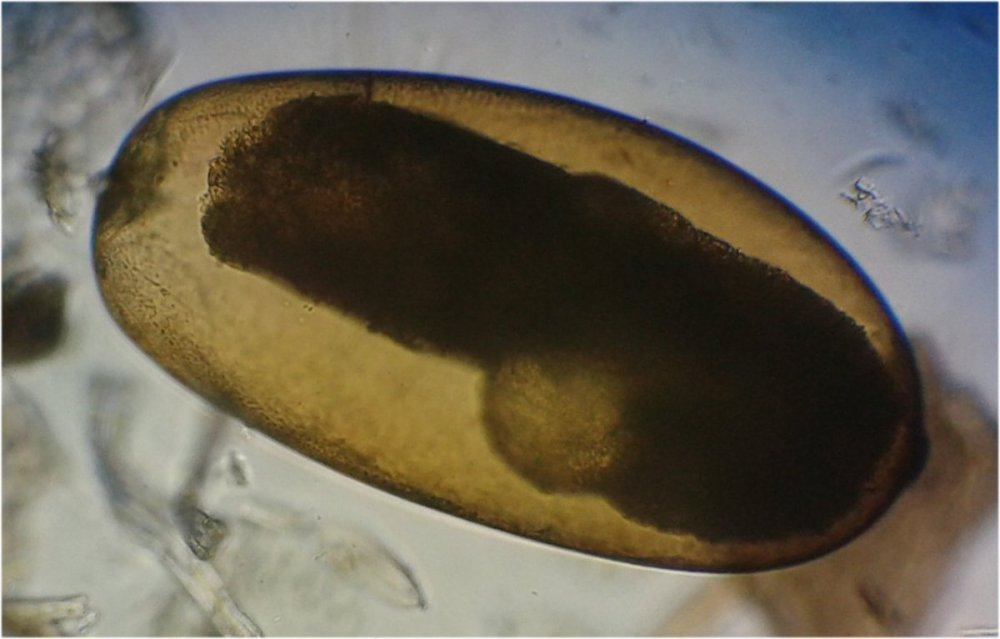
Un objet inattendu qui rappellerait un œuf
Sur des thèmes voisins de cette « coprologie aviaire » voir aussi :
https://forum.MikrOscOpia.com/topic/17024-fiente-de-pic-vert/#comment-67569
Amitiés
JMC
-
Il fait trop chaud pour aller chercher des échantillons, mais parfois ceux ci tombent littéralement du ciel !
En effet tous les matins des hirondelles tournent dans ma cour, se posent sur les fils à linge, gazouillent à tue tête, et parfois, en s’envolant, laissent un petit cadeau :
Voici donc sur une feuille du figuier une fiente qui mesure environ 1,5 cm.
En la diluant dans de l’eau , surtout la zone foncée, révèle un grand nombre de parties d’insectes. Sachant que les oiseaux n’ont pas de dents on peut s’interroger sur ce qui permet d’obtenir de si petits morceaux. Je pense que leur gésier doit contenir des particules de sable qui permettent la mastication.
N’étant pas entomologiste pour deux sous, je ne m’avancerai pas sur l’identification des insectes ingérés, mais contrairement à ce qu’on pense ce ne sont pas que des moustiques !
Il peut être utile d’utiliser une mini goutte de liquide vaisselle pour aider à mouiller les morceaux de kératine . A défaut d’identification on peut toutefois regrouper les structures par fonctions . Sauf mention contraire les images sont faites au x 15 :
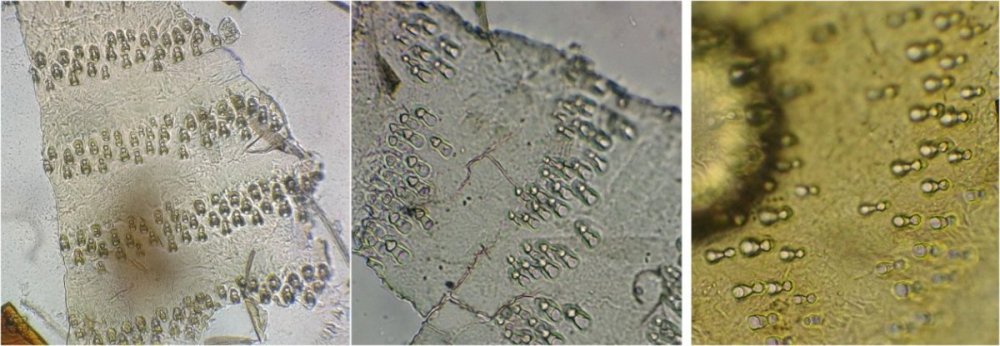
Les écailles d’ailes : on remarque la présence d’écailles longues et fines provenant certainement d’ailes de moustiques mais aussi d’autres types d’écailles :
Des fragments d’ailes où l’on distingue les pédicelles d’attache des écailles
Voir ici : https://forum.MikrOscOpia.com/topic/19533-%C3%A9caille-des-papillons/#comment-81091
Des pattes difficiles à identifier car très morcelées
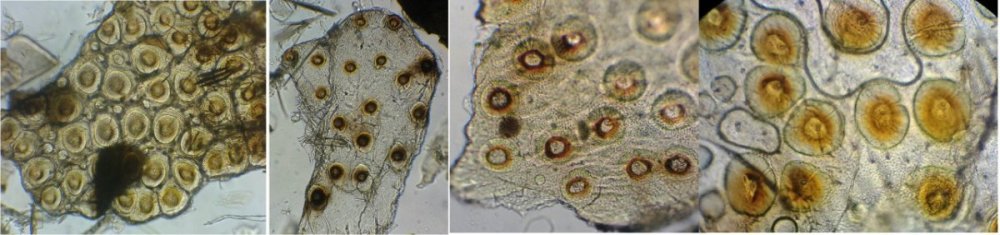
des cornées faciles à reconnaître par leurs éléments hexagonaux
des fragments d’épiderme ou d’élytres avec des ornementations circulaires et des poils aux centre de chacune
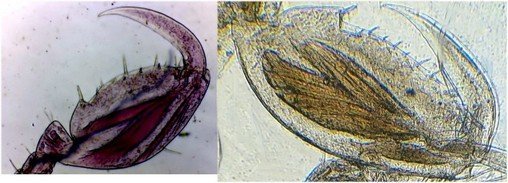
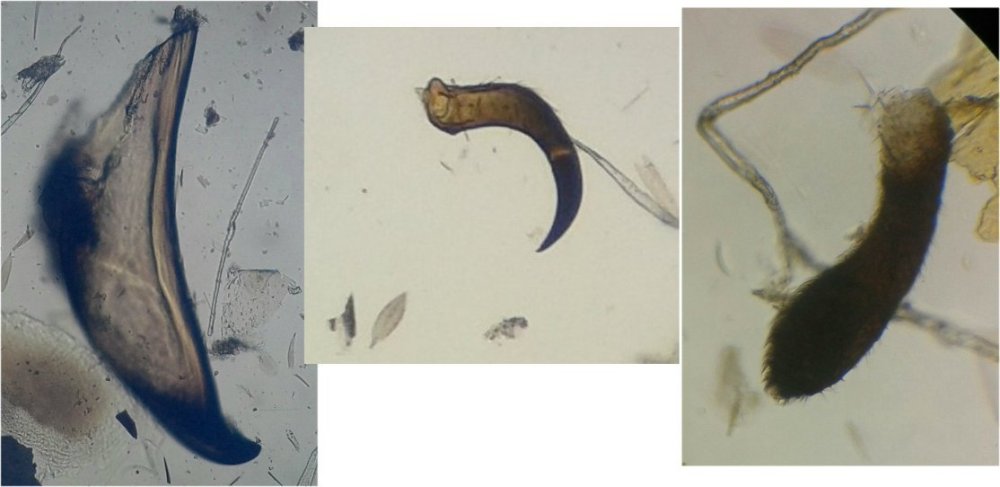
des griffes / mandibules / palpes
-
Bonjour à tous
Jean Marc , on peut utiliser le LM338 qui va à 3 A ce qui est largement suffisant pour des Leds . Pour calculer le courant dans R1 la formule est 1,25/R1. (R1 en ohms). L'inconvénient est que toute l'intensité va passer par le rhéostat R1 qui doit tenir le coup... ça se trouve des rhéostats 2 W mais c'est un peu cher.Je préconiserait un commutateur 6 positions commutant des résistances de puissance (entre 1 et 2 w) sachant que c'est rare qu'on ait besoin d'un réglage très fin de la lumière...*
Je peux faire un schéma si besoin
Amitiés
JMC
* J'ai une alim simplifiée pour led 1 W avec 2 positions : Normal et Boost cette dernière position n'étant utilisée que pour le X 40
-
Bonjour
En analogique il y a le LM338 K qui peut aller jusqu'à 5 ampères (3 A pour 338 sans K) et son montage en générateur de courant ci dessous.. On doit pouvoir remplacer R1 par un commutateur de plusieurs résistance supportant les intensités demandée; on n'a pas forcément besoin d'un réglage fin...

Amitiés
JMC
-
Bonjour
vu sur ce site plusieurs types de radiateurs et même certains ventilés de petite taille . pour une LED 3 watts que l'on n'utilise pas toujours à pleine puissance cela doit suffire...Pour l'alimenter en courant continu c'est moins évident, les drivers "tout fait" sortent en courant alternatif....
Amitiés
JMC
-
Bonjour
Je voudrais attirer l'attention sur le fait que ces petits modules d'alimentation ne sont pas des générateurs de courant . Une faible variation du réglage de la tension peut faire varier dans de grandes proportions le courant dans la led . voir ici
https://www.microscopies.com/DOSSIERS/Magazine/Articles/JMC-LEDS-2/LEDS2.htm
A défaut un fusible en série avec la LED me parait indispensable : par exemple pour LED 3 watts fusible 1,5 A, pour 10 watts 3,15 A ou 4 A etc...
Amitiés
JMC
-
Bonjour Jean Luc
Moi c'est Jean-Marie (pas Jean Marc ! )
Le problème principal pour la LED c'est de pouvoir la positionner à la place de l'ampoule actuelle. Bien que la LED soit plus petite , il faut aussi loger son radiateur indispensable. Pour une remplacer une ampoule de 30 w on peut estimer qu'une LED 3 W (qui consomme 1 ampère) est suffisante. Les alims pour LEDS disponibles travaillent en courant constant mais en alternatif ! Il faut concevoir une alimentation filtrée en courant continu ou utiliser une alimentation de laboratoire réglable en courant.
Il faudrait avoir une photo de l'ampoule en place pour voir si la transformation (réversible) est possible
Pour Neat Image le principe est de prendre un échantillon de bruit seul sur une zone unie de l'image et de faire son spectre en fréquence puis le soustraire de l'Image. Probablement en utilisant la transformée de Fourier. Mais si on peut d'emblée obtenir une bonne image le post processing est inutile.
AMitiés
JMC
-
Bonjour Jean Luc
Vraiment intéressante ta démarche , que l'on pourrait aussi appliquer au zooplancton vivant et qui m'intéresse à ce titre !.
Pour le scintillement (et les barres sur les images) la solution serait de passer en éclairage LED alimenté en courant continu filtré , il pourrait être même possible au moment de la prise de vue de suralimenter brièvement la LED pour faire un pseudo flash (comme sur les téléphones) .
Pour le bruit on peut utiliser Neat image dont voici le résultat avec la version gratuite et en prenant comme échantillon un rectangle en haut à droite de l'image:

Amitiés
JMC
-
Bonjour Dominique
L'algue filamenteuse n'est pas une cyanobactérie... Je pense à Geminella peut être , mais je ne suis pas très riche en algues d'eau douce !
Amitiés
JMC
-
-
Bonjour Dominique
Bonne initiative ! c'est intéressant de pouvoir suivre les populations au cours de l'année . On dirait que les premières images de la série sont en contraste de phase ? avec une certaine perte de résolution par rapport au fond clair me semble-t-il ...
En parlant d'estran cela m'a rappelé ce site qui décrit pas mal d'espèces :
https://nature22.com/estran22/estran.html
Amitiés
JMC
-
Bonjour
Lors de l'identification du copépode paracartia grani Lien ci dessous
https://forum.MikrOscOpia.com/topic/20108-reproduction-du-copépode-paracartia-grani/#comment-83424
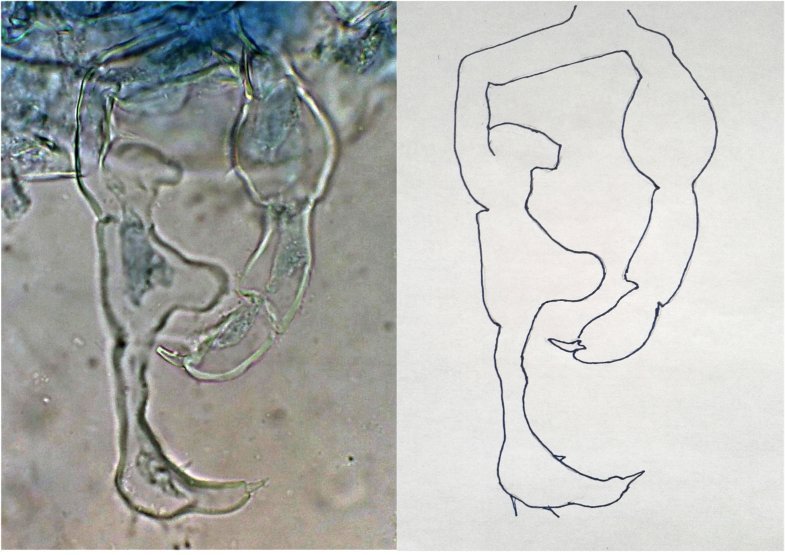
L'identification avait été facilitée par sa pince (P5) :

en reprenant une autre lame voici une nouvelle pince qui parait utiliser le même principe et permet d'identifier l'espèce : Acartia clausi de la même famille que le précédent . (Image au x 40)

Une photo du mâle : ce n'est pas sa pince qui est un peu cachée (flèche) mais celle d'un autre spécimen : (Image au x 6,3). L'antenne géniculée est celle de gauche sur l'image

Pour l'instant je n'ai pas identifié la femelle mais il doit y en avoir sur la lame.
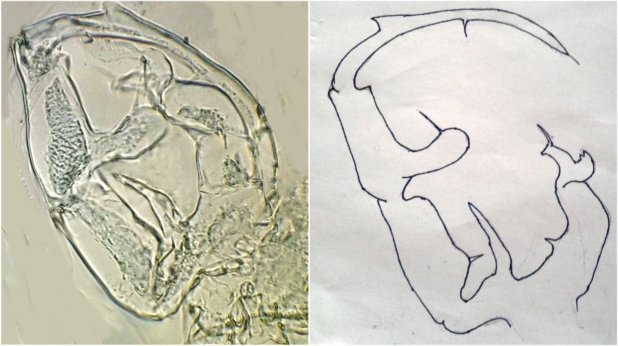
Identification grâce a "M.ROSE(Faune de France 26)Copepodes-pelagiques". J'en profite pour rendre hommage à tous ces scientifiques, qui ne disposant pas de moyens photos aussi pratiques que les nôtres, ont réalisé à la main les dessins des détails d'identification !
Amitiés
JMC
-
Bonjour
Une image que j'ai retrouvée sur une autre lame montrant l'antennule géniculée pliée dans la position qui maintien la femelle :

Amitiés
JMC
-
Bonjour
Allez je tente Colpidium ?
http://protist.i.hosei.ac.jp/pdb/images/ciliophora/colpidium/index.html
Amitiés
JMC















.jpg.b10e939d859152a3e8b4e84a1184543e.jpg)








Qui fait encore des lames montées ?
dans - Préparations microscopiques
Posté(e)
Bonjour
J'ai oublié une précision importante : au vu des images on pourrait croire que la conservation (image en 2026) améliore la qualité d'image ! En fait la photo de 2004 est prise avec caméra vidéo analogique champ de 384x282 pixels , l'image finale étant compositée (manuellement) à partir de plusieurs images élémentaires alors que celle de 2026 est prise à 5 méga pixels directement....
Amitiés
JMC